- Article
- Source : Campus Sanofi
- 17 juin 2022
Connaître et reconnaître une inflammation de type 2

L’inflammation de type 2 : un phénotype clinique fréquent
L’asthme est une maladie inflammatoire hétérogène présentant des phénotypes cliniques variés (âge de survenue, sexe, obésité, tabagisme…) et des endotypes, liés aux mécanismes physiopathologiques sous-jacents.
On distingue l’inflammation de type 2 (T2) impliquant les lymphocytes T2 et les cellules lymphoïdes innées de type 2 (ILC2), et l’inflammation non T2 ou neutrophilique, définie par la présence de 40 à 60 % de neutrophiles dans les expectorats.1 L'endotype paucigranulocytaire, moins fréquent, ne présente pas d'inflammation cellulaire notable dans les voies respiratoires. Constatée chez un patient, elle devrait inciter à reconsidérer le diagnostic de l'asthme.1
L'inflammation de type 2 est retrouvée chez 50 à 70 % des patients asthmatiques.2-3
Comment distinguer un asthme d’inflammation de type 2 vs. non type 2 ?
L'inflammation de type 2 est caractérisée par :
• une surproduction des IL-4, IL-5 et IL-131
• une importante production d'IgE et d'éosinophiles1
• un important remodelage bronchique4
• une réponse positive aux corticothérapies4-5
• un risque accru de faire des exacerbations et des atopies4-6
L'inflammation non-type 2. Plus rares, ces endotypes sont caractérisés par :
• un asthme d’apparition tardive6
• la présence de neutrophiles6
• peu ou pas d'éosinophiles1-7
• une faible réponse aux corticoïdes4-7
• une association à l'obésité et au tabagisme7
• une obstruction et une hyperréactivité bronchique moins évidentes que dans l'endotype de type 26
Les cytokines IL-4, IL-5 et IL-13 au coeur de l’inflammation de type 2 ?
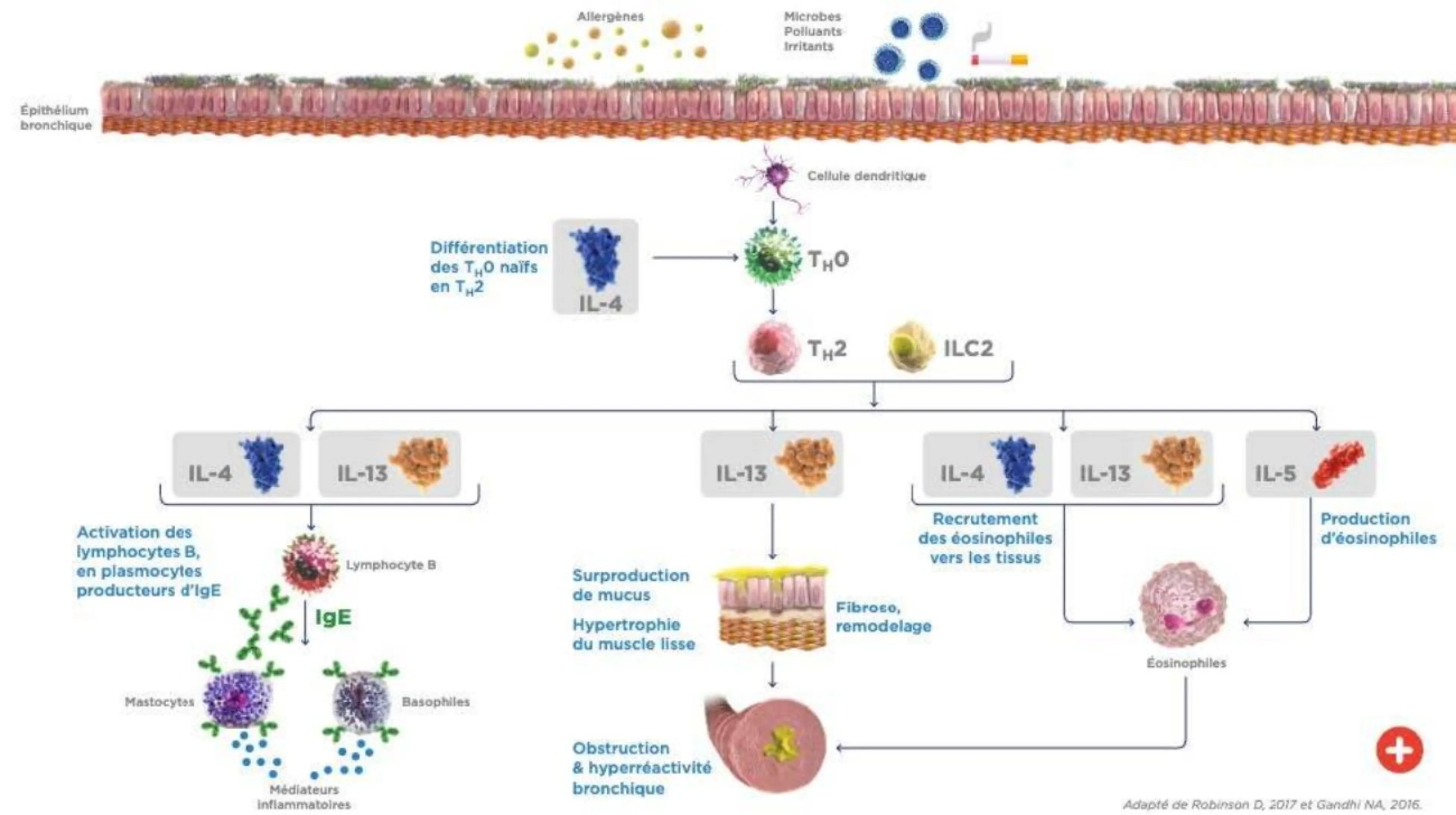
L'inflammation de type 2 est caractérisée par des cytokines, en particulier les IL-4, IL-5 et IL-13, produites en partie par des lymphocytes Th2 et des ILC2 suite à la reconnaissance d'allergènes.1-8 Ces cellules peuvent également être activées par les IL-33, IL-25 et la lymphopoïétine stromale thymique (TSLP) produites par les cellules épithéliales bronchiques après exposition à des virus, des bactéries ou des irritants.8
Cette cascade a plusieurs effets :
• La production d'IgE par les lymphocytes B sous l'action de l'IL-4.1
• L'activation des mastocytes, qui provoquent une contraction des muscles lisses, une infiltration d'éosinophiles, un remodelage et une amplification de la cascade inflammatoire par une production supplémentaire d'IL-3, IL-4, IL-5 et IL-9.1
• La maturation et l'activation des éosinophiles par l'intermédiaire de l'IL-5, et leur recrutement par le IL-4 et IL-13.1-9
• Une hyperréactivité et une hypertrophie du muscle lisse par l'IL-13.1
Comment reconnaître l'inflammation de
type 2 ?
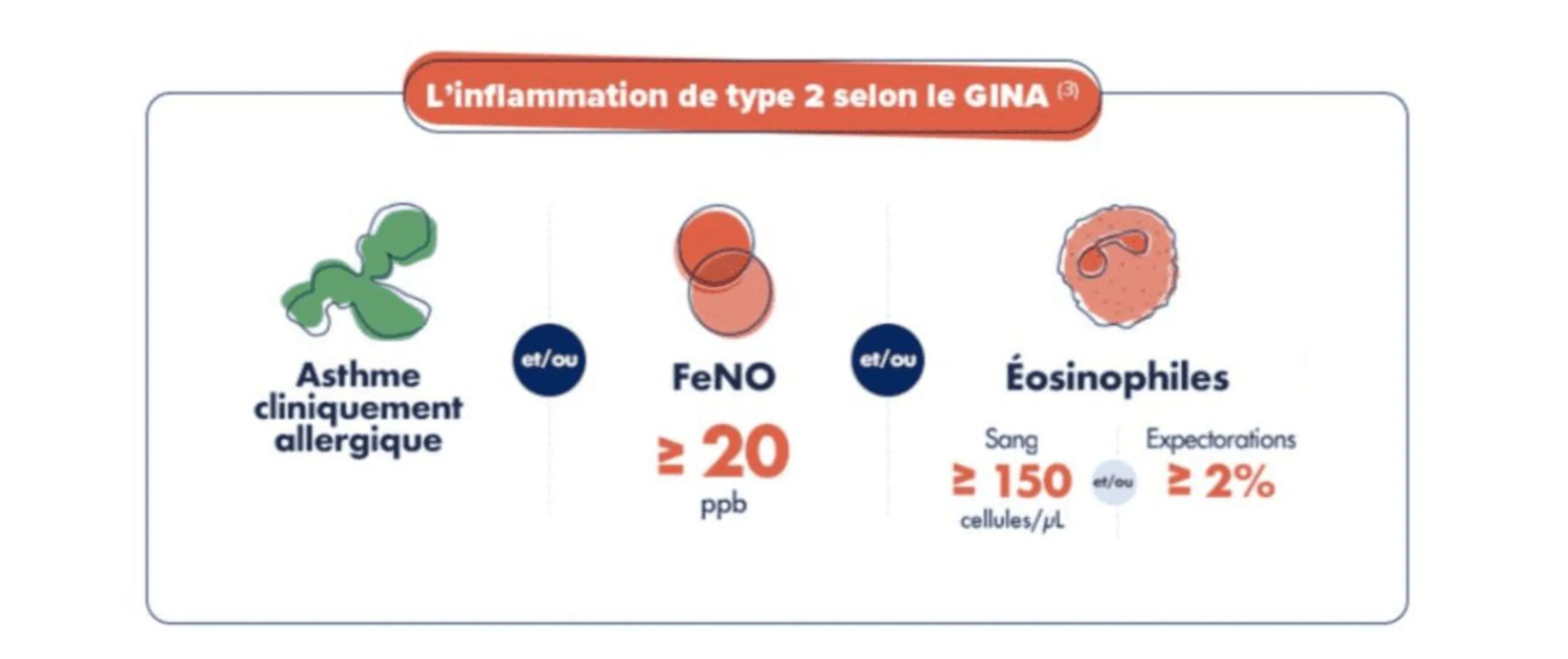
L'inflammation de type 2 est caractérisée par au moins un des éléments suivants8 :
• l'asthme est cliniquement allergique
• un taux d'éosinophiles :
○ d'au moins 150/μl dans le sang
○ d'au moins 2 % dans les expectorations
• une FeNO d'au moins 20 ppb
Il faudra répéter l'évaluation des éosinophiles sanguins et de la FeNO jusqu'à trois fois, sous la dose de corticoïdes la plus basse possible.8
Points clés
• L'inflammation de type 2 concerne 50 à 70 % des patients atteints d'asthme sévère.
• Elle est caractérisée par la production d'interleukines 4, 5 et 13, ainsi que la production d'IgE et de l'activation et du recrutement d'éosinophiles.
• La FeNO, les éosinophiles ou l'aspect cliniquement allergique de l'asthme permettent de repérer les inflammations de type 2.
Références
- Israel E, Reddel HK. N Engl J Med. 2017;377 : 965-76.
- Peters MC, et al. J Allergy Clin Immunol. 2014;133(2) : 388–394.
- Seys SF, et al. Respiratory Research. 2017;18 : 39.
- Colas L, et al. Front. Medicine. 2020;7 : 98.
- Robinson D, et al. Clin Exp Allergy. 2017;47(2) : 161-75.
- Wenzel SE. Nature Medicine. 2012;18(5) : 716-25.
- Kuruvilla ME, et al. Clin Rev Allergy Immunol. 2019; 56(2) : 219–233.
- Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention, 2022. Available from : www.ginasthma.org.
- Gandhi NA, et al. Nat Rev Drug Discov. 2016;15(1) : 35-50.
7000038524 - 06/2022