Des objectifs adaptés aux patients atteints de PNS : le cas de Pierre
- Article
- Campus Sanofi
- 13 nov. 2023
Rencontre avec Pierre, 57 ans, atteint de polypose naso-sinusienne sévère*.
Lire plusRéservé aux professionnels de santé en France

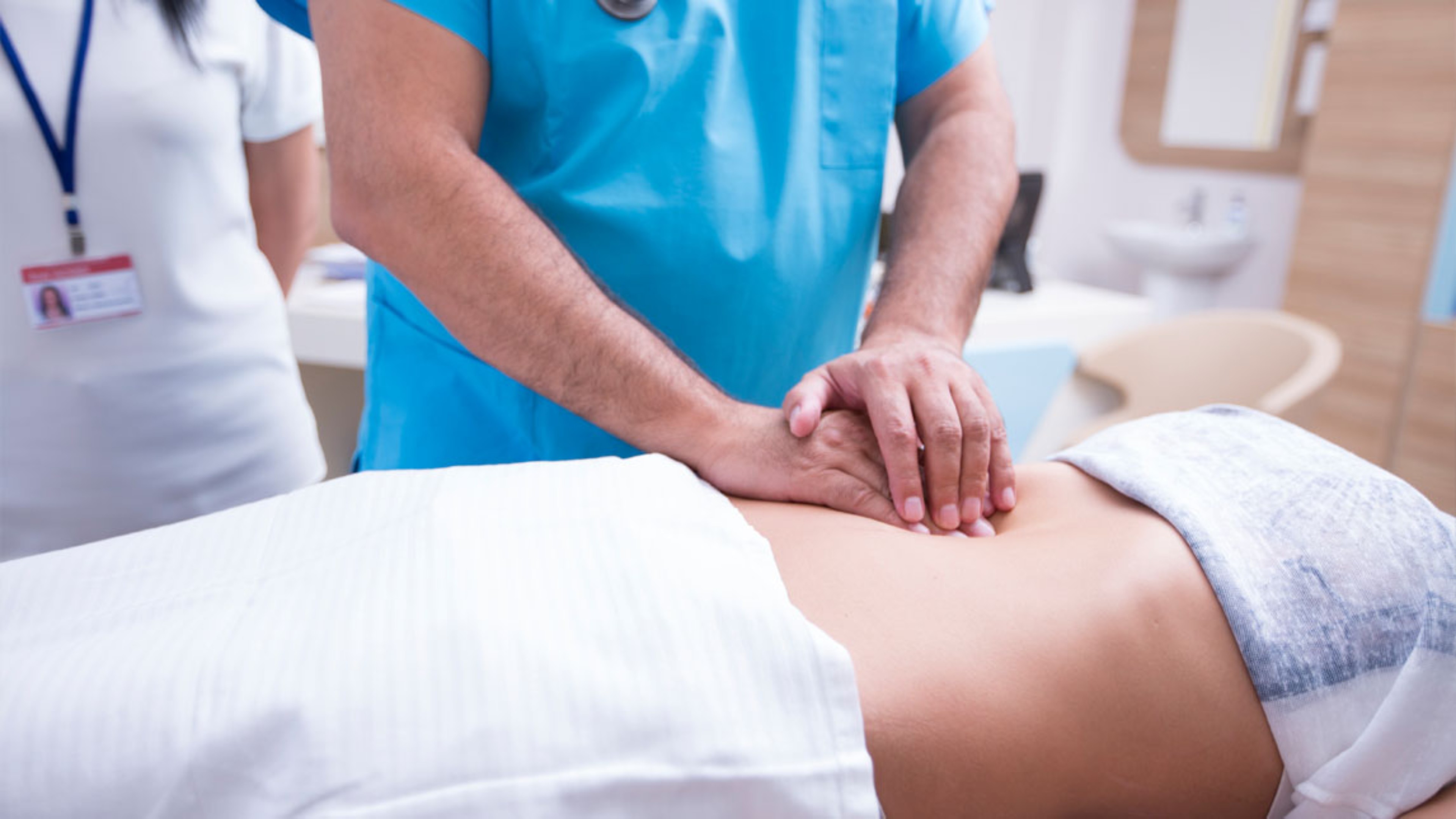
Explorez en 5 minutes les Techniques Essentielles pour une Palpation Précise et Informative avec le Pr Marc Michel
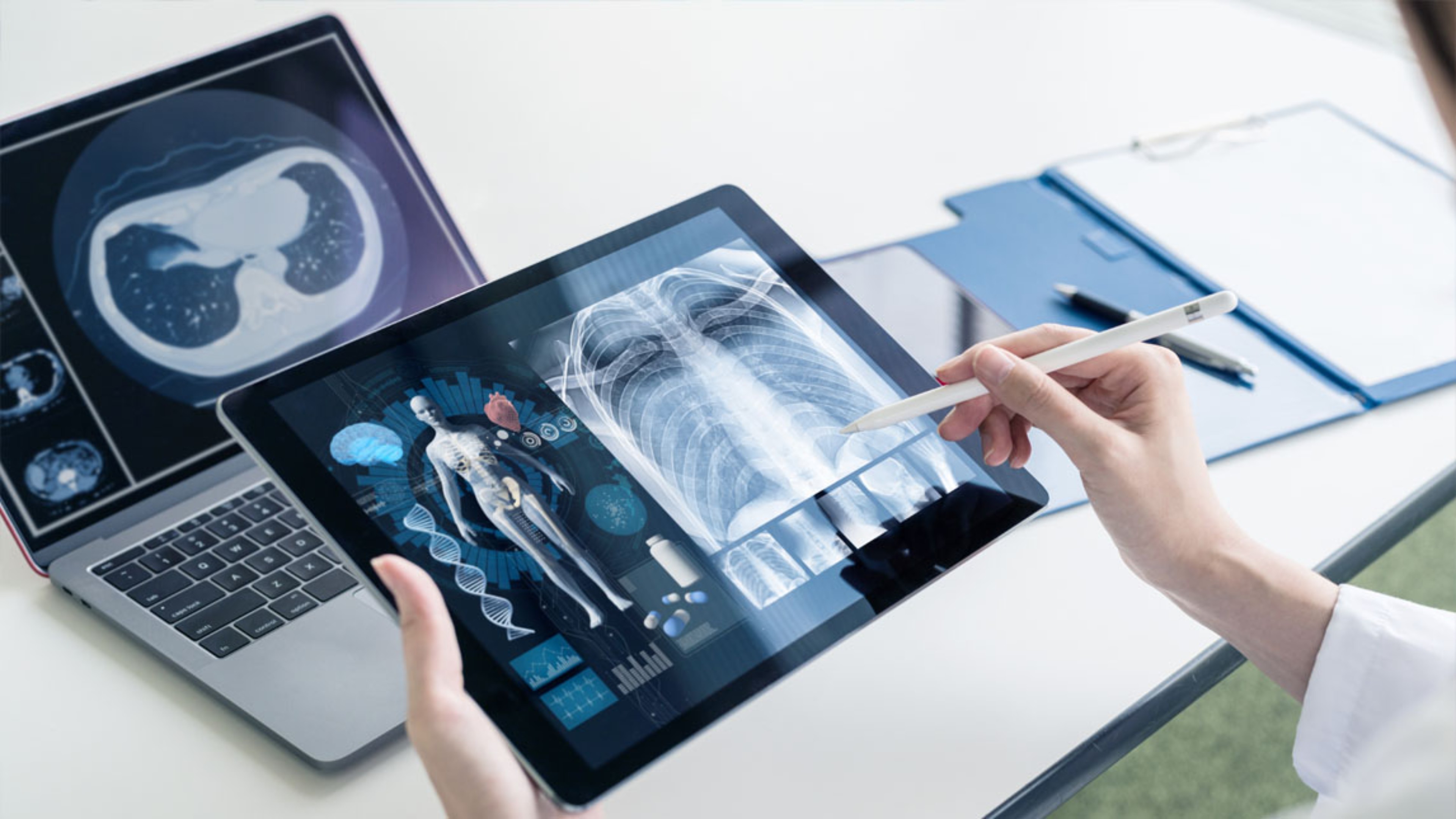
Découvrez le replay du symposium présenté par le Dr. Bertrand LIOGER, lors de la 87e édition du congrès de la SNFMI à Paris, explorant les signes d’appels de l’ASMD tels que la Splénomégalie et la Pneumopathie Interstitielle Diffuse (PID).

Découvrez le replay du symposium présenté par le Pr Vincent COTTIN, lors de la 28e édition du congrès du CPLF, sur la démarche diagnostique de la Pneumopathie Interstitielle Diffuse (PID) et ses diagnostics différentiels.